Ученые долго не понимали, как тело чувствует холод: ответ нашли в термодинамике нервных рецепторов
Способность живых организмов ощущать температуру окружающей среды — одна из базовых функций нервной системы, особо важная для выживания. У млекопитающих за распознавание холода отвечает специфический мембранный белок TRPM8. Это ионный канал, расположенный в окончаниях соматосенсорных нервных волокон. Он активируется при падении температуры ниже 26 °C, а также при контакте с некоторыми химическими соединениями, наиболее известным из которых является ментол.
Функциональная роль TRPM8 изучена достаточно подробно: когда температура снижается, канал открывается, пропуская внутрь нервной клетки ионы кальция. Это изменение электрического потенциала мембраны генерирует импульс, который передается в головной мозг и интерпретируется как ощущение холода. Однако до недавнего времени базовая биофизика этого процесса оставалась скрытой от науки. Исследователи не могли точно описать, каким образом физическое снижение температуры (то есть уменьшение кинетической энергии в системе) заставляет массивную молекулу белка изменить свою форму и открыть пору.

Группа исследователей под руководством молекулярных биологов Дэвида Джулиуса (лауреата Нобелевской премии за открытие температурных рецепторов) и Ифаня Чэна опубликовала в научном журнале Nature работу, которая детально описывает этот механизм. Ученые продемонстрировали, что для понимания работы температурных рецепторов недостаточно просто знать их статичную форму — необходимо изучать их термодинамику и подвижность в естественной среде.
Ограничения традиционных методов структурной биологии
Исторически главным инструментом для изучения формы белков является криоэлектронная микроскопия (крио-ЭМ). Стандартный протокол этого метода требует извлечения белка из клеточной мембраны. Для этого используются детергенты — химические вещества, которые растворяют мембрану, изолируя целевой белок. Затем очищенный образец резко замораживают и сканируют пучком электронов.
В случае с рецептором TRPM8 этот метод регулярно давал неполные результаты. Проблема заключается в самой природе термочувствительного белка. Чтобы реагировать на малейшие колебания температуры, TRPM8 должен обладать высокой структурной подвижностью. Он не имеет одной жесткой формы, а постоянно переходит из одного состояния в другое. Из-за этой динамики на получаемых микроскопических изображениях область самой поры — той части, которая должна открываться и закрываться — всегда оставалась размытой.
Вторая проблема заключалась в использовании детергентов. Растворяя мембрану, ученые удаляли все сопутствующие клеточные липиды. Как выяснилось позже, эти липиды не просто окружают рецептор, а принимают непосредственное участие в его физической активации.
Чтобы преодолеть эти ограничения, авторы нового исследования принципиально изменили подход. Во-первых, они отказались от детергентов и изучали TRPM8 прямо внутри клеточных везикул — микроскопических фрагментов настоящей клеточной мембраны, сохранивших все естественные липиды.
Во-вторых, в дополнение к крио-ЭМ ученые применили метод водород-дейтериевого обмена в сочетании с масс-спектрометрией (HDX-MS). Суть этого метода заключается в измерении гибкости различных участков белка. Молекулу помещают в раствор с тяжелой водой, в которой вместо обычного водорода содержится его тяжелый изотоп — дейтерий. В тех участках белка, которые отличаются гибкостью и подвижностью, атомы водорода быстро заменяются на дейтерий. В участках с жесткой, стабильной структурой этот обмен происходит крайне медленно. Анализируя массу различных фрагментов белка при разных температурах (от 37 °C до 4 °C), исследователи смогли точно определить, какие части рецептора становятся жесткими при охлаждении, а какие сохраняют подвижность.
Механика открытия: от жесткости к движению
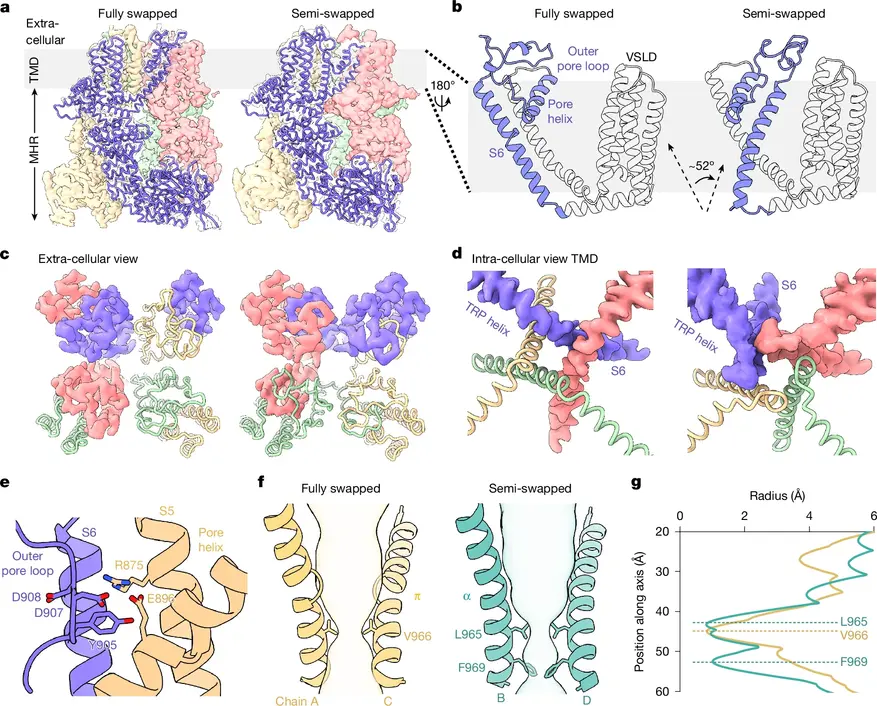
Объединив данные микроскопии и масс-спектрометрии, ученые обнаружили, что рецептор TRPM8 существует в двух основных структурных конфигурациях. Белок состоит из четырех одинаковых субъединиц, которые вместе образуют центральную пору. В классическом состоянии, которое ученые назвали «полностью переплетенным», элементы одной субъединицы плотно взаимодействуют с соседней.
Однако исследователи зафиксировали и второе, ранее неизвестное состояние — «полупереплетенное». В этой конфигурации ключевой структурный элемент белка, так называемая трансмембранная спираль S6, изгибается примерно на 52 градуса и меняет свое положение, возвращаясь к собственному домену, а не связываясь с соседним. Ионный канал находится в состоянии динамического равновесия, постоянно переключаясь между этими конфигурациями.
Анализ HDX-MS показал точную последовательность событий при снижении температуры. Когда окружающая среда охлаждается, внешняя часть поры рецептора резко теряет свою подвижность и становится термодинамически жесткой. Это изменение распространяется по структуре белка и физически воздействует на спираль S6, заставляя ее изменить свое положение.
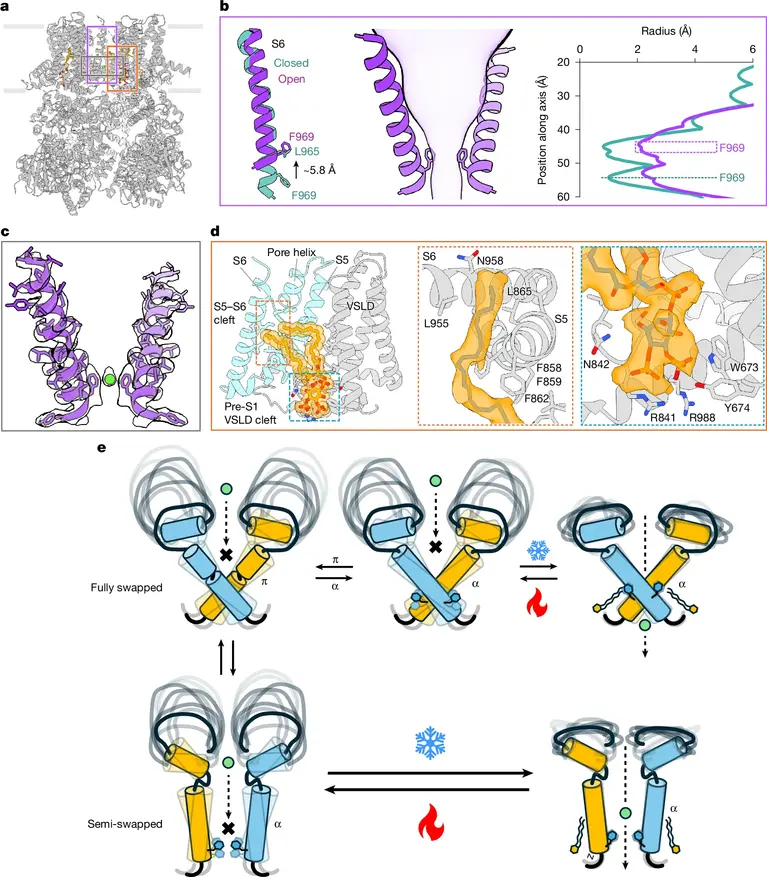
Смещение спирали S6 приводит к образованию в структуре белка небольшой гидрофобной полости. Именно на этом этапе становится понятна роль клеточной мембраны. В образовавшуюся полость проникает длинный углеводородный хвост молекулы PIP2 (фосфатидилинозитол-бисфосфата) — липида, который всегда присутствует в мембране клетки. Липид фиксирует спираль S6 в новом положении, не позволяя ей вернуться обратно.
Это структурное смещение достигает самого низа ионного канала, где расположена крупная аминокислота фенилаланин (F969). Под давлением сместившейся спирали молекула фенилаланина меняет свою пространственную ориентацию, отгибаясь вверх. В результате центральное отверстие канала расширяется. Ионы кальция получают возможность беспрепятственно пройти через мембрану внутрь клетки, что и приводит к генерации нервного импульса.
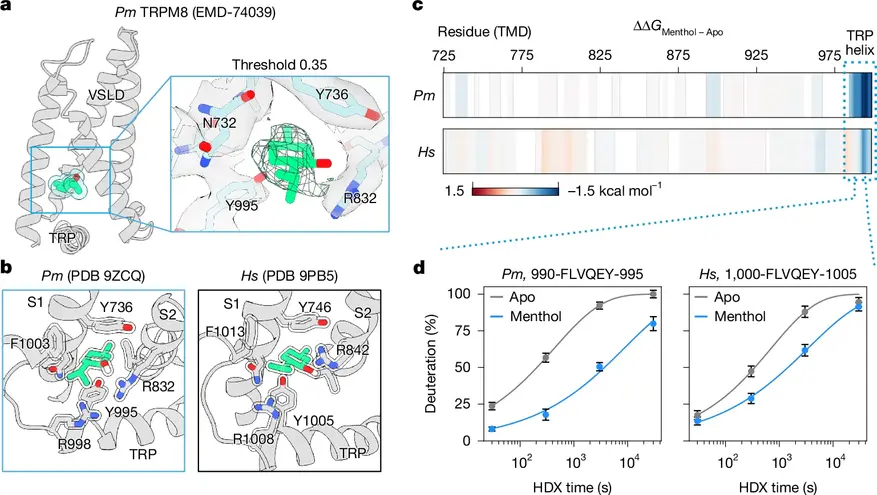
Действие ментола приводит к аналогичному результату, но инициируется в другой части белка. Ментол связывается с нижним доменом рецептора, стабилизируя соседнюю спираль (TRP-спираль). Это изменение также приводит к смещению спирали S6 и последующему открытию поры при участии липида PIP2.
Эволюционная биология: почему птицы не чувствуют холод
Детальное понимание структуры TRPM8 позволило исследователям объяснить давний физиологический парадокс, связанный с терморегуляцией птиц. Известно, что птицы, в отличие от млекопитающих, обладают крайне низкой чувствительностью к холоду. Они могут длительное время находиться на льду или снегу без признаков температурного дискомфорта в конечностях.
Сравнение генетических последовательностей показало, что рецепторы TRPM8 у птиц и человека идентичны на 92%. Их трехмерные структуры практически неотличимы друг от друга. Однако их реакция на снижение температуры принципиально разная.
Исследователи локализовали причину этого различия во внешней части поры. У человека и других млекопитающих в строго определенной позиции (V915) находится аминокислота валин. У птиц в аналогичной позиции (Y905) располагается аминокислота тирозин.
Структурный анализ показал, что молекула тирозина у птиц вступает в сильное химическое взаимодействие с окружающими заряженными аминокислотами. Эта химическая связь жестко фиксирует птичий рецептор в закрытом, «полупереплетенном» состоянии. Энергетический барьер, который необходимо преодолеть для изменения формы этого белка, оказывается очень высоким. Простого снижения температуры окружающей среды (которое работает у млекопитающих) физически недостаточно, чтобы разорвать эти связи и вызвать смещение спирали S6. Пора остается закрытой, и нервный сигнал не генерируется. У млекопитающих валин не образует таких сильных стабилизирующих связей, оставляя рецептор готовым к активации при охлаждении.
Для подтверждения этой гипотезы ученые провели прямой генетический эксперимент. Они внесли точечную мутацию в ген человеческого рецептора TRPM8, заменив валин на тирозин. Полученный измененный человеческий рецептор полностью утратил способность реагировать на холод, начав вести себя как белок птицы. В обратном эксперименте исследователи заменили тирозин на валин в птичьем гене. Клетки, экспрессирующие такой измененный птичий рецептор, начали активно генерировать кальциевые сигналы в ответ на снижение температуры.
Этот эксперимент демонстрирует, как в процессе эволюции всего одна аминокислотная замена в структуре белка, состоящего из тысяч атомов, способна радикально изменить физиологические характеристики целого класса позвоночных животных, обеспечив им адаптацию к различным климатическим условиям.
Заключение
Для полного понимания того, как рецептор реагирует на внешние стимулы, недостаточно зафиксировать его форму — необходимо измерить его энергетический ландшафт и проследить изменение подвижности каждого сегмента.
Физиологическое ощущение холода оказалось прямым следствием локального изменения энтальпии специфического участка белка, что запускает строгую геометрическую трансформацию всей молекулы.
Источник: Nature











0 комментариев
Добавить комментарий