Эволюция не отнимала у нас способность к регенерации: биологи доказали, что млекопитающие могут восстанавливать конечности с нуля
Вопрос, почему одни животные способны отращивать оторванные конечности, а другие — нет, занимал еще Аристотеля. Спустя две тысячи лет эволюционная биология сформировала довольно пессимистичный консенсус для нашего вида: млекопитающие променяли регенерацию на теплокровность, сложный иммунитет и защиту от генетических ошибок. В ходе эволюции наш класс животных выработал другую стратегию выживания: при серьезной травме организм стремится как можно быстрее закрыть рану, чтобы предотвратить потерю крови и проникновение инфекции. Для этого используется грубая соединительная ткань. Возникает быстрое рубцевание, или фиброз, который надежно запечатывает повреждение, но делает невозможным выращивание новой сложной структуры.
Однако новое исследование биологов из Техасского университета A&M и Тулейнского университета показывает, что эта биологическая программа вовсе не удалена из нашего генома. Она просто подавляется процессом рубцевания. Ученые доказали, что обычные клетки взрослого млекопитающего сохраняют полную информацию о том, как выстраивать сложные анатомические системы. Процесс регенерации можно запустить искусственно, если в правильной последовательности изменить химическую среду внутри раны.

Анатомическая граница: почему палец не растет сам
В качестве экспериментальной модели исследователи использовали мышей, которым ампутировали палец на уровне второй фаланги. Эта область выбрана не случайно: биологи давно знают, что у мышей (как и у людей) способность к естественной регенерации строго зависит от уровня повреждения. Если ампутация затрагивает только самый край фаланги, где находится ногтевое ложе, ткани способны восстановиться самостоятельно. Но если разрез проходит глубже, через сустав или кость второй фаланги, организм запускает процесс фиброза. Рана просто зарастает кожей и соединительной тканью, образуя обычную культю.
У земноводных на месте любой ампутации немедленно формируется специфическая структура — бластема. Это плотное скопление активно делящихся клеток. Чтобы создать бластему, клетки в области раны проходят через процесс дедифференцировки. Они теряют свою узкую рабочую специализацию (перестают быть клетками мышц, кожи или костей) и возвращаются в раннее, неспециализированное состояние, похожее на состояние клеток эмбриона. Из этого скопления затем формируются все необходимые для новой конечности ткани.
У млекопитающих быстрое формирование рубца физически и химически блокирует этот процесс. Задачей биологов было найти способ остановить образование шрама и заставить клетки культи пойти по пути формирования настоящей бластемы.
Первый этап: остановка рубцевания и накопление клеток
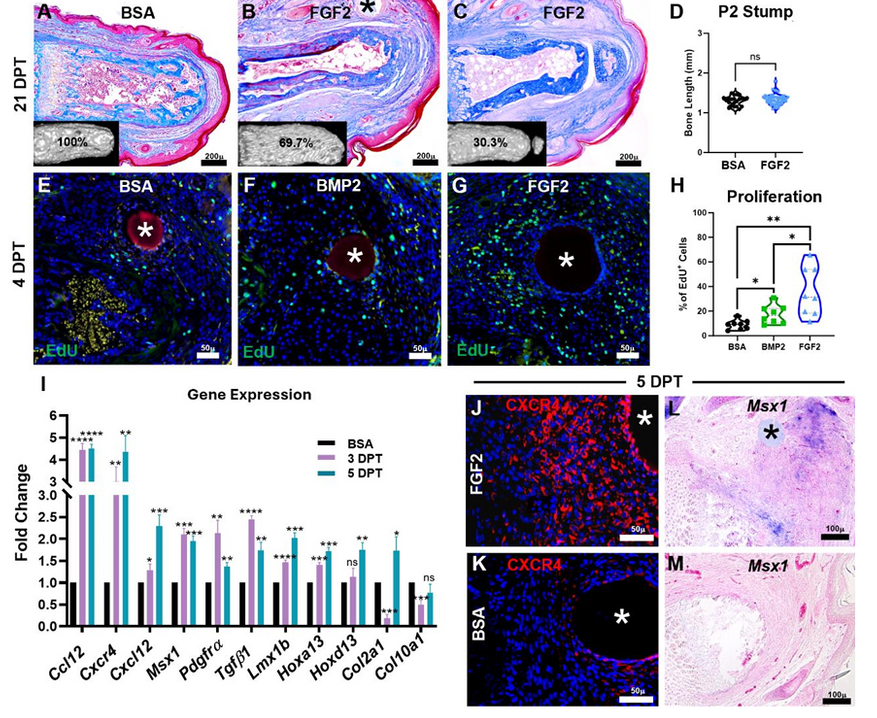
Чтобы изменить поведение клеток в ране, исследователи применили специфическую сигнальную молекулу — фактор роста фибробластов 2 (FGF2). На четвертый день после ампутации они поместили микроскопические гранулы, пропитанные этим белком, прямо в центр нерегенерирующей раны.
FGF2 кардинально изменил процесс заживления. Он подавил формирование рубцовой ткани и заставил фибробласты (основные клетки соединительной ткани, которые обычно и формируют шрам) вести себя иначе. Они начали активно делиться и накапливаться на конце культи.
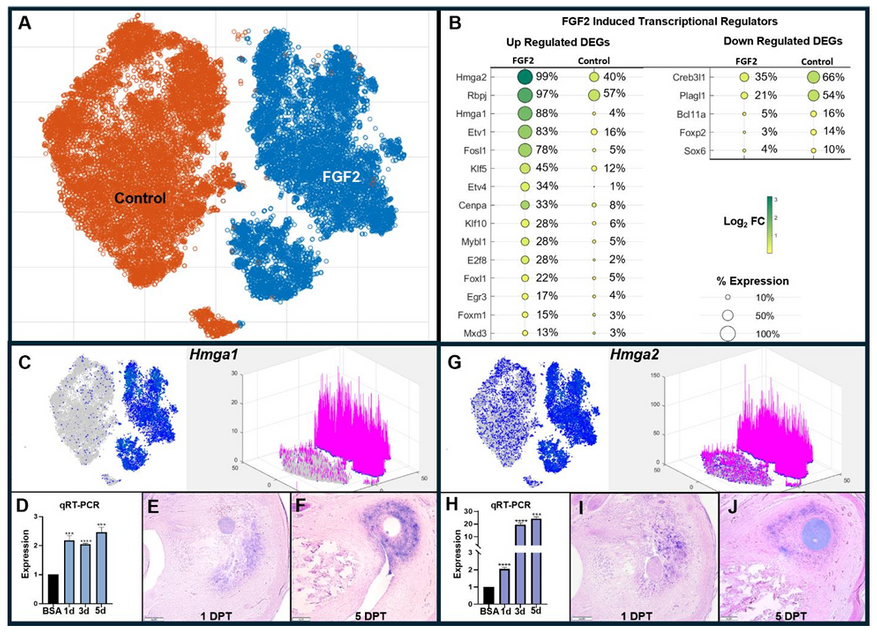
Ученые провели анализ матричной РНК этих клеток и обнаружили, что в них резко возросла активность генов Hmga1 и Hmga2. Эти гены в норме активны на стадии эмбрионального развития, когда организм только формирует свои пропорции и структуры. Их включение у взрослой мыши означало, что клетки действительно утратили свою первоначальную функцию и вернулись в базовое состояние. На конце культи образовалась настоящая бластема.
Но на этом этапе эксперимент столкнулся с проблемой. FGF2 инициировал сбор неспециализированных клеток, но не давал им дальнейших инструкций. Без дополнительных химических стимулов скопление клеток не понимало, в какие именно ткани ему нужно превращаться. Бластема просто поддерживала свое существование некоторое время, не формируя костей или хрящей, а затем постепенно распадалась.
Второй этап: дифференцировка и формирование скелета
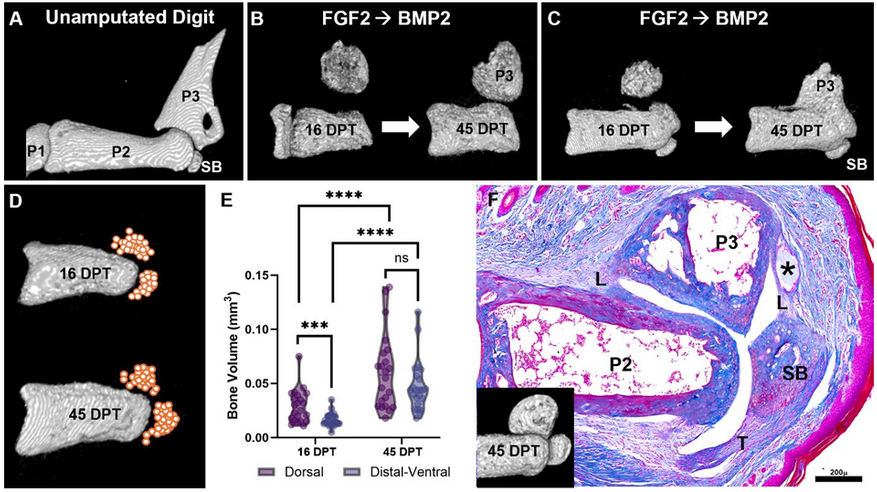
Чтобы направить клетки бластемы по пути формирования полноценного скелета, потребовался второй химический сигнал — костный морфогенетический белок 2 (BMP2). Этот белок отвечает за развитие костных и хрящевых структур. Основным фактором успеха стала строгая временная последовательность: BMP2 вводили в рану ровно через пять дней после применения первого белка.
Такая последовательная стимуляция привела к полному формированию утраченных структур. Под воздействием BMP2 клетки бластемы начали превращаться в хондроциты (хрящевые клетки) и запустили процесс эндохондрального окостенения. Это биологический механизм, при котором организм сначала создает хрящевой макет будущей кости, а затем постепенно замещает его твердой костной тканью. Именно так растут кости конечностей в период внутриутробного развития.
У экспериментальных мышей полностью регенерировала удаленная третья фаланга. Новая кость имела правильную анатомическую форму, внутри нее образовался полноценный костномозговой канал, а снаружи появились естественные места для крепления связок. Одновременно с этим восстановились сесамовидная кость (небольшая кость, расположенная в толще сухожилий) и сустав с синовиальной полостью, обеспечивающей подвижность.
Отслеживание судьбы клеток и пространственная память
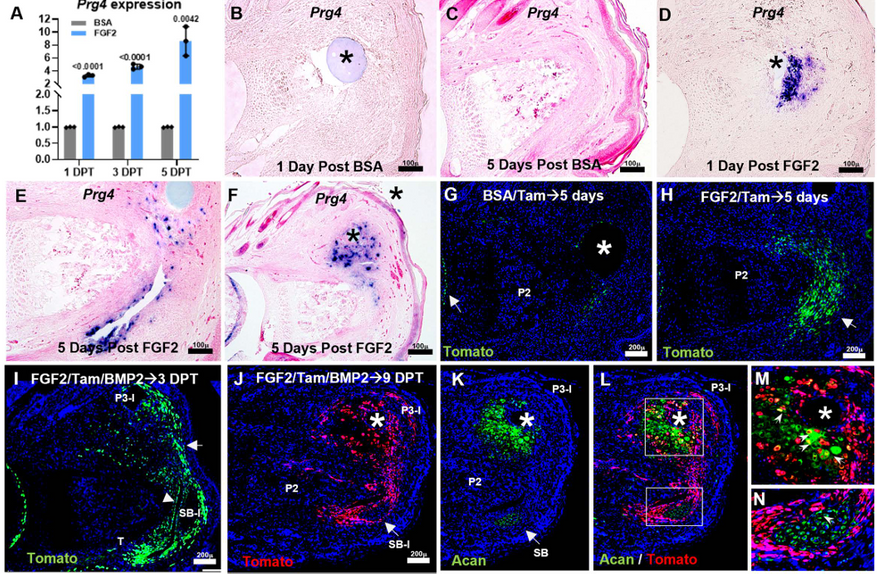
Чтобы убедиться, что новые ткани действительно образовались из клеток раны, а не из каких-либо других источников, биологи применили метод генетического маркирования. Они пометили специальным светящимся маркером клетки, экспрессирующие ген Prg4. В обычных условиях этот ген работает в клетках, которые выстилают поверхность суставов и выделяют суставную смазку.
Наблюдения показали хорошую пластичность этих клеток. Под воздействием двух введенных белков клетки, которые в норме просто сформировали бы суставную оболочку или рубец, вошли в состав бластемы и превратились в хрящевые и костные клетки новой фаланги.
Более того, исследование подтвердило наличие у клеток млекопитающих пространственной памяти. Клетки второй фаланги, из которых образовалась бластема, точно знали, что им нужно выстроить именно третью фалангу и сустав, а не дублировать вторую фалангу заново. Это явление в биологии называется дистальной трансформацией, и ранее считалось, что он полноценно функционирует только у земноводных.
Перспективы для регенеративной медицины
Выходит что обычные клетки, которые ежедневно участвуют в банальном заживлении порезов и травм, обладают достаточным биологическим потенциалом, чтобы заново выстроить сложную систему из костей, хрящей и связок.
Единственная разница между формированием рубца у мыши (или человека) и отращиванием новой лапы у саламандры заключается в биохимическом составе микроокружения раны в первые дни после травмы. Млекопитающим физически не хватает специфических сигнальных молекул, чтобы вовремя остановить фиброз и запустить эмбриональную программу.
Успех с последовательным введением белков FGF2 и BMP2 показывает, что управление поведением клеток в ране абсолютно реально. Это открывает новый вектор развития для регенеративной медицины. В будущем восстановление утраченных тканей или даже частей конечностей может достигаться не за счет сложной пересадки стволовых клеток, выращенных в лаборатории, а за счет точечной химической стимуляции собственных резервов организма прямо в месте повреждения.
Источник: researchgate











16 комментариев
Добавить комментарий
а если создать условия изолированные от заражений, не давать организму закрывать рану кожей, и запускать туда 2 белка, один сначала для создание каркаса из хрящей, второй через некоторое время для укрепления этого каркаса уже костной тканью, то конечность вырастит также, как прописано в днк. Дальше уже процесс сам пойдёт, прирост тканей, мыщц, кожи. Это будет прорыв в медицине
Одно не понятно, что с кровью, как его остановить, если рана большая
Ну большие раны уже зашивают, там, конечно речи наверное быть и не может о том чтобы руку, например, отрастить. Хотя палец же тоже зашивают. В общем, на бумаге то все хорошо и гладко, а как в реальности это будет работать на ком-то крупном, вроде человека, я пока представить себе не могу
Прямо как в «5 элементе» ;)
Проще говоря — они не лезут в биос и ядро системы(как делали ученые по омоложению ранее, что приводило к генным ошибкам и онкологии), а лишь меняют настройки в ОС.
Добавить комментарий